A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nesta terça-feira (20) o uso emergencial de um medicamento contra a Covid-19. Trata-se de um coquetel que contém a combinação de casirivimabe e imdevimabe (Regn-CoV2), dois remédios experimentais desenvolvidos pela farmacêutica Roche. É o segundo medicamento aprovado pela agência. O primeiro foi o remdesivir.
O que é o Regn-CoV2 e como ele será administrado:
- Os medicamentos devem ser administrados juntos por infusão intravenosa;
- O coquetel é composto por dois anticorpos monoclonais (casirivimabe e imdevimabe) que bloqueiam a entrada do vírus na célula;
- O tratamento é indicado para adultos e pacientes pediátricos (com 12 anos ou mais que pesem no mínimo 40 kg) que não necessitam de suplementação de oxigênio;
- Ele não é recomendado para pacientes graves;
- Ele não é indicado para prevenção da Covid-19;
- O coquetel já foi aprovado para uso emergencial nos Estados Unidos, Canadá e Suíça. Também teve recomendação de uso pela agência europeia de medicamentos (EMA);
- Ele não substitui as vacinas contra a Covid-19.


Anvisa aprova uso emergencial de medicamento contra Covid
A aplicação é intravenosa e o medicamento é indicado para o começo da doença. O uso é restrito a hospitais e a venda é proibida ao comércio.
“Esses produtos são o que a gente chama de anticorpos monoclonais. A ideia dessa proposta é neutralizar o vírus para que ele não se propague nas células infectadas e assim controlar a doença”, explica o gerente geral de medicamentos e produtos biológicos, Gustavo Mendes.
Segundo a Anvisa, o tratamento é indicado para adultos e pacientes pediátricos (com 12 anos ou mais que pesem no mínimo 40 kg) que não necessitam de suplementação de oxigênio, com infecção por SARS-CoV-2 confirmada por laboratório e que apresentam alto risco de progressão para Covid-19 grave.
O medicamento não é recomendado para pacientes graves. “Anticorpos monoclonais como casirivimabe e imdevimabe podem estar associados a piora nos desfechos clínicos quando administrados em pacientes hospitalizados com Covid-19 que necessitam de suplementação de oxigênio de alto fluxo ou ventilação mecânica”, alerta a Anvisa.
O pedido de uso emergencial foi feito no dia 1º de abril.
/i.s3.glbimg.com/v1/AUTH_59edd422c0c84a879bd37670ae4f538a/internal_photos/bs/2021/j/y/cKIrZKSBGSKMIGOEVY6Q/ap21028559039124.jpg)
/i.s3.glbimg.com/v1/AUTH_59edd422c0c84a879bd37670ae4f538a/internal_photos/bs/2021/j/y/cKIrZKSBGSKMIGOEVY6Q/ap21028559039124.jpg)
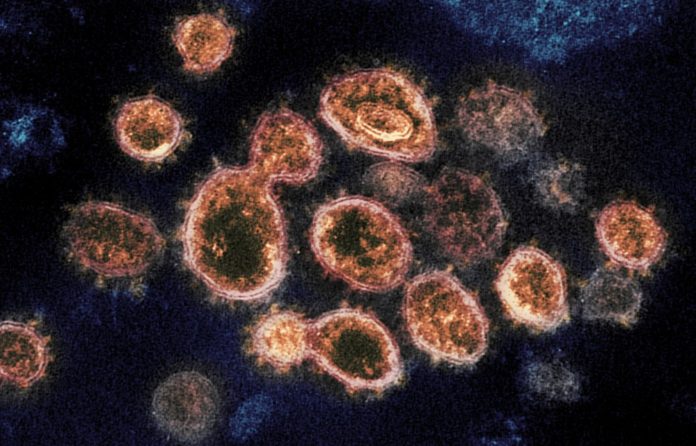
Imagens de microscópio mostram partículas do coronavírus que causam a Covid-19 retiradas de um paciente nos EUA — Foto: NIAID-RML via AP
Aprovado em outros países
O coquetel já foi aprovado para uso emergencial pela FDA, agência de saúde dos Estados Unidos, após apresentar bons resultados em pacientes com sintomas leves e moderados da Covid-19. Ele também foi usado no tratamento do ex-presidente americano Donald Trump.
Segundo o órgão americano, a combinação “reduziu a hospitalização relacionada a Covid-19 ou as visitas ao pronto-socorro em pacientes com alto risco de progressão da doença em 28 dias após o tratamento, quando comparados ao placebo”.
O medicamento também foi aprovado para uso emergencial no Canadá, Suíça e teve recomendação de uso pela agência europeia de medicamentos (EMA).
Remdesivir
Em março, a Anvisa anunciou o registro do primeiro medicamento para pacientes hospitalizados com Covid-19, o antiviral remdesivir, que ainda está em estudos.
O Remdesivir é produzido pela biofarmaceutica Gilead Sciences e o seu nome comercial é Veklury. Trata-se de um medicamento sintético administrado de forma intravenosa (injetado na veia). Ele age impedindo a replicação viral.
O gerente geral de Medicamentos e Produtos Biológicos da Anvisa, Gustavo Mendes, esclareceu que o remdesivir não é vendido em farmácia e pode ser utilizado apenas com supervisão médica. “É uso restrito pelos hospitais para que os pacientes possam ser adequadamente monitorados”, disse.